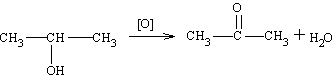Aldehydy i ketony
Aldehydy i ketony są pochodnymi węglowodorów zawierającymi charakterystyczną grupę funkcyjną
 , zwaną grupą karbonylową.
Gdy jedna z dwóch wartościowości atomu węgla grupy karbonylowej związana jest z grupą organiczną, a druga z atomem wodoru mamy wzór cząsteczki aldehydu, a gdy obie wartościowości węgla związane są z grupami organicznymi mamy wzór cząsteczki ketonu
, zwaną grupą karbonylową.
Gdy jedna z dwóch wartościowości atomu węgla grupy karbonylowej związana jest z grupą organiczną, a druga z atomem wodoru mamy wzór cząsteczki aldehydu, a gdy obie wartościowości węgla związane są z grupami organicznymi mamy wzór cząsteczki ketonu

Podstawnikiem w grupie karbonylowej może być zarówno grupa alkilowa jak i wrylowa. Z tego względu wyróżniamy aldehydy i ketony alifatyczne i aromatyczne. Aldehydy i ketony wykazują pewne różnice w reaktywności, szczególnie w reakcjach ich utleniania i przyłączenia do grupy karbonylowej. Różnice w reaktywności, szczególnie w reakcjach ich utleniania i przyłączenia do grupy karbonylowej. Różnice te uwarunkowane są liczbą, wielkością orach charakterem podstawników alkilowych lub arylowych.
Nazwa aldehyd wywodzi się od łac. "alcohol dehydrogenatus" - czyli alkohol odwodorniony; określenie to pochhodzi stąd, że aldehydy można otrzymać przez odrywanie atomów wodoru od alkoholi. Ogólną nazwę keton wyprowadzono od najprostszego przedstawiciela tego szeregu połączeń - acetonu. Z uwagi na fakt, że aldehydy brdzo lątwo utleniają się do kwasów karboksylowych, nazwy potoczne aldehydów wywodzą się od nazw kwasów, które można otrzymać przez ich utlenienie; mówi się zatem o aldehydzie mrówkowym HCHO, octowym CH3CHO, masłowym C3H7CHO, benzoesowym C6H5CHO. Nazwy potoczne ketonów tworzy się od nazw podstawników, np. keton dimetylowy, etylowometylowy itp. Według zasad słownictwa systematycznego IUPAC grupy aldehydowe
 oznacza się końcówką -al, a grupy ketonowe
oznacza się końcówką -al, a grupy ketonowe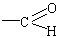 końcówką -on. Tworząc nazwę aldehydu (według słownictwa racjonalnego) wybieramy najdłuższy łańcuch w cząsteczce zawierający grupę aldehydową -CHO. Łańcuch ten numerujemy rozpoczynając od grupy aldehydowej, która z natury rzeczy musi znajdować się na końcu łańcucha. Obecność grupy aldehydowej zaznaczamy za pomocą przyrostka -al. Położenia oraz rodzaj podstwników zaznaczamy w zwykły sposób. Poniżej przedstawiam nazwy zwyczajowe i systematyczne przykładowych aldehydów.
końcówką -on. Tworząc nazwę aldehydu (według słownictwa racjonalnego) wybieramy najdłuższy łańcuch w cząsteczce zawierający grupę aldehydową -CHO. Łańcuch ten numerujemy rozpoczynając od grupy aldehydowej, która z natury rzeczy musi znajdować się na końcu łańcucha. Obecność grupy aldehydowej zaznaczamy za pomocą przyrostka -al. Położenia oraz rodzaj podstwników zaznaczamy w zwykły sposób. Poniżej przedstawiam nazwy zwyczajowe i systematyczne przykładowych aldehydów.
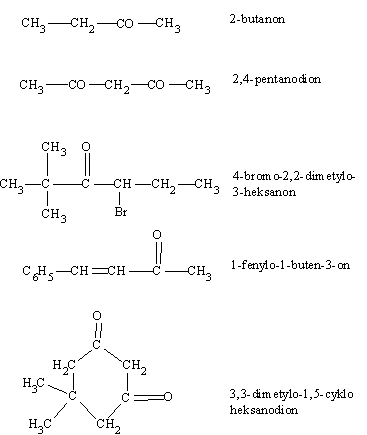
Tworząc racjonalną nazwę ketonu wybieramy najdłuższy łańcuch węglowy zawierający grupę karbonylową. Jej położenie w łańcuchu określa liczba dana na początku nazwy. W przypadku ketonów zawierających dwie lub trzy grupy karbonylowe stosujemy końcówkę dion lub trion i za pomocą dwu lub trzech cyfr określamy położenie tych grup. Przykłady wzorów i nazw aldehydów i ketonów zawierających więcej grup karbonylowych przedstawiam poniżej:
Temperatury wrzenia aldehydów i ketonów o podobnej masie cząsteczkowej są zbliżone do siebie, jednak nieco wyższe niż odpowiadających im węglowodorów, a znacznie niższe niż odpowiednich alkoholi. Aldehydy o większej masie cząsteczkowej mają dość przyjemny zapach szczególnie takie aldehydy aromatyczne, jak aldehyd benzoesowy i cynamonowy (C6H5-CH=CH-CHO). Również ketony mają zwykle przyjemny zapach i są bardziej odporne na utlenianie niż aldechydy. Niektóre ketony o małych masach cząsteczkowych są dobrymi rozpuszczalnikami żywic i lakierów, a aldehydy mrówkowy i octowy są ważnymi odczynnikami przemysłowymi. Wodny roztwór aldehydu mrówkowego, tzw. formalina jest stosowany do konserwowania preparatów biologicznych
Powstawanie
Najczęściej stosowaną i najważniejszą metodą otrzymywania aldehydów jest łagodne utlenianie alkoholi pierwszorzędowych, a ketonów - utlenianie alkoholi drugorzędowych
 Powstający w pierwszym etapie rekcji utleniania aldehyd, jest bardziej wrażliwy na środki utleniające niż wyjściowy alkohol i utlenia się dalej do kwasu karboksylowego.
Gdyby końcowy wynik utleniania zależał jedynie od reaktywności chemicznej obu substratów, wówczas otrzymywanie aldehydów przez utlenianie alkoholi byłoby niemożliwe. Wykorzystuje się tu jednak większą lotność aldehydu, przez szybkie usuwanie wytworzonego aldehydu z mieszaniny reagującej zapobiega się jego dalszemu utlenianiu.
teoretycznie ciekawe jest spostrzeżenie, że alkohol utlenia się także do aldehydu bez udziału tlenu, jeżeli stusuje się jego odwodorowanie, np. za pomocą palladu
Powstający w pierwszym etapie rekcji utleniania aldehyd, jest bardziej wrażliwy na środki utleniające niż wyjściowy alkohol i utlenia się dalej do kwasu karboksylowego.
Gdyby końcowy wynik utleniania zależał jedynie od reaktywności chemicznej obu substratów, wówczas otrzymywanie aldehydów przez utlenianie alkoholi byłoby niemożliwe. Wykorzystuje się tu jednak większą lotność aldehydu, przez szybkie usuwanie wytworzonego aldehydu z mieszaniny reagującej zapobiega się jego dalszemu utlenianiu.
teoretycznie ciekawe jest spostrzeżenie, że alkohol utlenia się także do aldehydu bez udziału tlenu, jeżeli stusuje się jego odwodorowanie, np. za pomocą palladu
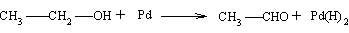 Ketony są bardziej odporne na działanie środków utleniających w porównaniu z aldehydami. Można je łatwo otrzymać przez utlenienie alkoholi drugorzędowych bez konieczności stosowania specjalnych środków ostrożności.
Ketony są bardziej odporne na działanie środków utleniających w porównaniu z aldehydami. Można je łatwo otrzymać przez utlenienie alkoholi drugorzędowych bez konieczności stosowania specjalnych środków ostrożności.
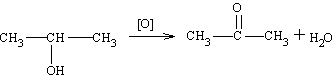 Synteza ta jest jednocześnie dowodem budowy chemicznej ketonów. Podobnie jak w przypadku aldehydów, ketony można otrzymywać również przez odwodorowanie alkoholi drugorzędnych.
Jako środków utleniających podczas utleniania alkoholi pierwszo- lub drugorzędowych stosuje się tlne atmosferyczny wobec katalizatorów takich jak platyna lub miedź. W laboratoriach do utleniania używa się zwykle dwuchromianu i kwasu siarkowego. A oto przykłady równań reakcji utleniania alkoholu pierwszorzędnego do aldehydu dwuchromianem w środowisku kwaśnym. Współczynniki stechiometryczne i środowisko reakcji w równaniach można wydedukować stosują bilanś elektronowy, atomoty i ładunków.
Synteza ta jest jednocześnie dowodem budowy chemicznej ketonów. Podobnie jak w przypadku aldehydów, ketony można otrzymywać również przez odwodorowanie alkoholi drugorzędnych.
Jako środków utleniających podczas utleniania alkoholi pierwszo- lub drugorzędowych stosuje się tlne atmosferyczny wobec katalizatorów takich jak platyna lub miedź. W laboratoriach do utleniania używa się zwykle dwuchromianu i kwasu siarkowego. A oto przykłady równań reakcji utleniania alkoholu pierwszorzędnego do aldehydu dwuchromianem w środowisku kwaśnym. Współczynniki stechiometryczne i środowisko reakcji w równaniach można wydedukować stosują bilanś elektronowy, atomoty i ładunków.
 Równanie reakcji utleniania alkoholu drugorzędowego do ketonu wyprowazamy w podobny sposób
Równanie reakcji utleniania alkoholu drugorzędowego do ketonu wyprowazamy w podobny sposób
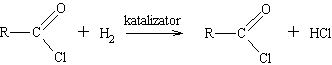
 Wygodną metodą przeprowadzania kwasu w aldehyd o tej samej liczbie atomów węgla w łańcuchu jest tzw. reakcja Rosenmunda. W metodzie tej kwas karboksylowy przeprowadza się w chlorek kwasowy, który następnie poddaje się katalitycznemu uwodornieniu do aldehydu.
Wygodną metodą przeprowadzania kwasu w aldehyd o tej samej liczbie atomów węgla w łańcuchu jest tzw. reakcja Rosenmunda. W metodzie tej kwas karboksylowy przeprowadza się w chlorek kwasowy, który następnie poddaje się katalitycznemu uwodornieniu do aldehydu.
Darmowy hosting zapewnia PRV.PL